Hoofdstuk 7
Warmte
§1 Temperatuur
In dit hoofdstuk gaan we fenomenen in de wereld om ons heen verklaren aan de hand van de beweging van kleine deeltjes waaruit de wereld bestaat. We noemen deze kijk op de wereld het deeltjesmodel. In deze eerste paragraaf gaan we de luchtdruk en de temperatuur op deze manier bestuderen.
De wereld bestaat uit kleine deeltjes die we atomen noemen. Hoewel atomen een miljoen keer kleiner zijn dan een millimeter - en dus niet met het blote oog te zien zijn - kunnen we ze tegenwoordig met goede microscopen wel waarnemen (zie de onderstaande linker afbeelding).
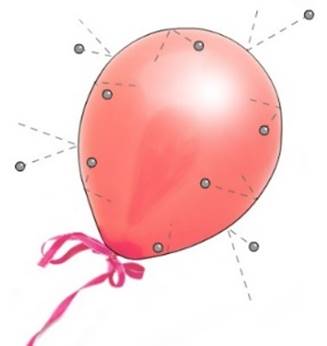
Veel fenomenen in de wereld om ons heen zijn te verklaren aan de hand van de beweging van atomen. We noemen deze methode om de wereld te begrijpen het deeltjesmodel. Een toegankelijk voorbeeld hiervan is de luchtdruk. De luchtdruk wordt veroorzaakt door het botsen van de miljarden atomen waaruit de lucht bestaat. We kunnen het effect van deze botsingen goed zien bij een opgeblazen ballon. Als je een ballon opblaast, dan pers je een hele hoop atomen de ballon in. Als een ballon opgeblazen is, dan is de kracht die de atomen op de binnenwand uitoefenen groter dan de kracht die de atomen op de buitenwand uitoefenen.

Ook de temperatuur kunnen we met het deeltjesmodel begrijpen. Zoals je weet meten we de temperatuur met een thermometer. Een veelgebruikte thermometer bestaat uit een dun buisje met daarin gekleurde alcohol (zie de onderstaande afbeelding). Als de alcohol warmer wordt, dan zet het uit, waardoor het alcoholniveau stijgt. Als de alcohol afkoelt, dan krimpt het, waardoor het alcoholniveau weer daalt.

De bekendste eenheid voor de temperatuur is de graden Celsius (°C). Het maken van een correcte schaal op een thermometer wordt het ijken van een thermometer genoemd. Dit doen we als volgt. Het alcoholniveau als we de thermometer in ijs steken noemen we 0 °C. Het alcoholniveau als we de thermometer in kokend water steken noemen we 100 °C. De afstand tussen deze twee niveaus kan dan in honderd gelijke stapjes van 1 °C verdeeld worden.
Ook de temperatuur wordt veroorzaakt door de beweging van de atomen waaruit het materiaal bestaat. Hoe sneller de atomen bewegen, hoe hoger de temperatuur van het voorwerp. Andersom geldt ook dat hoe langzamer de atomen bewegen, hoe lager de temperatuur wordt. Als we een voorwerp blijven afkoelen, dan komt er een moment dat alle atomen stil staan. Dit gebeurt bij -273 °C. Op dat moment is de allerlaagste temperatuur bereikt. We noemen deze temperatuur het absolute nulpunt. Het is niet mogelijk dat een materiaal nog kouder wordt, want de atomen staan op dit moment immers al helemaal stil.
Sinds de ontdekking van het absolute nulpunt wordt ook vaak een andere eenheid voor de temperatuur gebruikt: de kelvin (K). Bij deze schaal is ervoor gekozen om het absolute nulpunt 0 K te noemen. Er geldt dus:
|
… |
Het handige van deze schaal is dat de temperatuur in kelvin altijd positief is. Het kan immers niet kouder worden dan 0 K. Een ander voordeel is dat formules vaak simpeler worden als we gebruik maken van kelvin. Om deze redenen is de Kelvin de SI-eenheid voor de temperatuur. We rekenen kelvin en graden Celsius als volgt in elkaar om:
|
… |
T(K) staat voor de temperatuur in kelvin. T(°C) staat voor de temperatuur in graden Celsius.

Met het deeltjesmodel kunnen we ook meteen begrijpen waarom stoffen uitzetten als we de temperatuur verhogen en krimpen als we de temperatuur verlagen. Als we de temperatuur van bijvoorbeeld een stuk metaal verhogen, dan gaan de deeltjes in dit metaal sneller trillen. Door dit trillen duwt elke atoom de omliggende atomen een beetje weg. Het materiaal neemt op deze manier meer ruimte in.
In veel praktische situaties moeten we rekening houden met deze uitzetting. Bij veel bruggen zien we bijvoorbeeld een 'ritssluiting' (zie de linker onderstaande afbeelding). Dit zorgt ervoor dat de brug ruimte heeft om een beetje uit te zetten op een warme dag. In de rechter afbeelding zien we wat er gebeurt als er niet goed wordt nagedacht over de uitzetting van materialen. De rails in de afbeelding zijn helemaal kromgetrokken.

|
|
|
1. Noem de SI-eenheden van afstand, massa, volume en temperatuur.
1. Leg uit dat de temperatuur niet onder de -273°C kan komen.
2. Schrijf de volgende temperaturen om: a. 0 K = ... °C b. 473 K = ... °C c. 0 °C = ... K d. 100 °C = ... K
3. Schrijf de volgende temperaturen om: a. 125 K = ... °C b. 730 K = ... °C c. 200 °C = ... K d. -100 °C = ... K
4. Water kookt bij 100 °C, alcohol bij 351 K. Leg uit wat een hogere temperatuur heeft: kokend water of kokend alcohol?
5. Hiernaast zien we een afbeelding van een ongeijkte thermometer. De onderste stippellijn werd gezet toen de thermometer in ijswater gelegd werd. De bovenste stippellijn werd gezet toen de thermometer in kokend water gelegd werd. a. Noteer de schaalverdeling op de thermometer in stapjes van 10 °C. b. Welke temperatuur geeft de thermometer aan? c. Noteer de schaalverdeling ook in kelvin.
6. Hoe kan je de thermometer aanpassen zodat de afstand tussen elke graad Celsius groter wordt? Leg ook uit welk voordeel en welk nadeel deze grotere afstand heeft.
7. Twee veelgebruikte thermometers zijn buitenthermometers en koortsthermometers. Leg uit welke thermometer het grootste bereik heeft en welke de grootste nauwkeurigheid.
|
|
|
|
8. Leg met behulp van het deeltjesmodel uit waarom een vaste stof krimpt als de temperatuur afneemt.
9. Tussen de stukken van een betonnen wegdek zitten rubberen voegen. a. Waarom is dit gedaan? b. Leg uit of de voeg het breedst is in de zomer of in de winter.
10. Als je de verwarming aan zet, hoor je vaak krakende geluiden in het huis. Geef hiervoor een verklaring.
12. Op een spuitbus staat: 'LET OP!, niet blootstellen aan temperaturen boven de 50 graden Celsius'. Waarom mag dat niet?
13. Over een bekerglas wordt met een elastiekje een boterhamzakje strak gespannen. a. Wat gebeurt er met het zakje als we de beker verhitten? b. Wat gebeurt er met het zakje als we de beker in de koelkast zetten?
14. Een metalen dop is moeilijk van een glazen pot te draaien. Hoe los je dit probleem op met de theorie uit deze paragraaf?
|
§2 Faseovergangen
In deze paragraaf gaan we fasen en faseovergangen begrijpen met het deeltjesmodel.
Stoffen bevinden zich over het algemeen in één van de volgende drie fasen:
· gas
· vloeibaar
· vast
We kennen allemaal de drie fasen van water. Vast water noemen we ijs, vloeibaar water noemen we gewoon 'water' en water in gasvorm noemen we waterdamp.
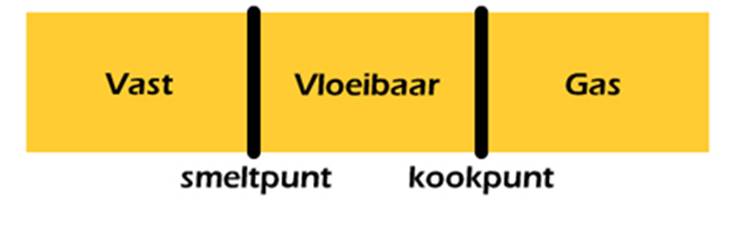
Een stof is vast als de temperatuur onder het smeltpunt ligt. Een stof is vloeibaar als de temperatuur tussen het smeltpunt en het kookpunt ligt en een stof is gasvormig als de temperatuur boven het kookpunt ligt (zie de onderstaande afbeelding).
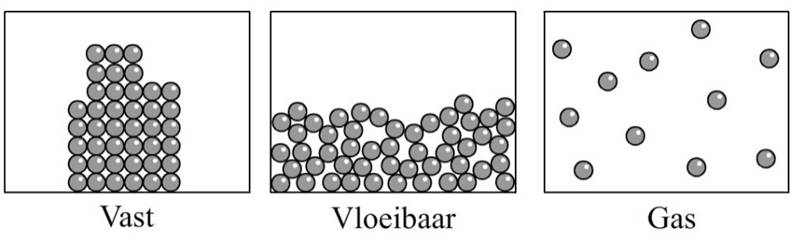
Ook deze drie fasen kunnen we met het deeltjesmodel begrijpen. Hieronder zien we de drie fasen op atomaire niveau afgebeeld. In de onderstaande linker afbeelding is een vaste stof op atomaire niveau afgebeeld. De atomen in een vaste stof zitten op een vaste plaats en kunnen op deze plaats alleen een beetje heen en weer trillen. Alleen bij 0 K staan de deeltjes helemaal stil.
Bij een vloeistof zitten de atomen nog steeds tegen elkaar aan, maar hebben ze geen vaste plek meer. Ze kunnen nu vrij langs elkaar heen bewegen (zie de middelste afbeelding). Dit verklaart de beweeglijkheid van vloeistoffen. In een gas zijn de atomen helemaal los van elkaar en vliegen kriskras door elkaar heen (zie de rechter afbeelding).
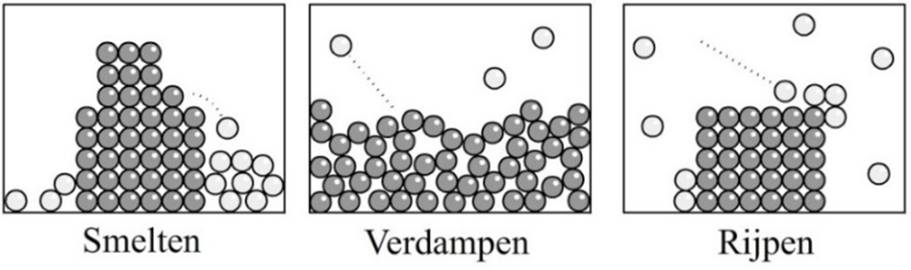
Als een stof van één fase overgaat naar een andere, dan spreken we van een faseovergang. Er zijn zes verschillende faseovergangen (zie de onderstaande afbeelding). Hieronder zien we bijvoorbeeld de overgang van vast naar vloeibaar (links) en van vloeibaar naar gas (midden). Zelfs een voorwerp zo hard als staal wordt bij hogere temperaturen een vloeistof (rechts).

Er bestaan zes verschillende faseovergangen:
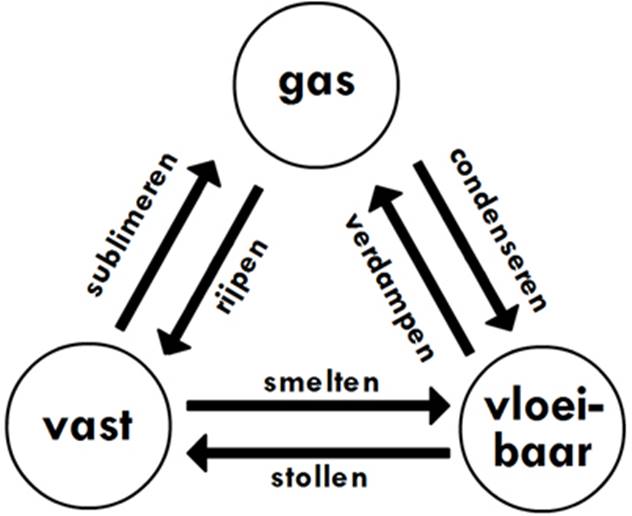
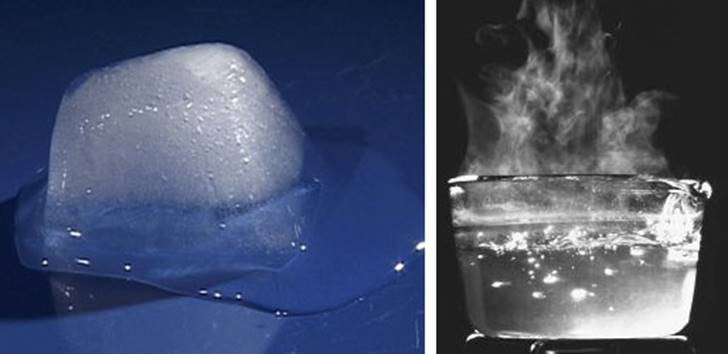
Als een vloeistof in een vaste stof verandert, dan noemen we dit stollen. Als een vaste stof in een vloeistof verandert, dan noemen we dit smelten. Water stolt als we het afkoelen onder de 0 °C en smelt als we het verwarmen boven de 0 °C. We noemen 0 °C daarom het smeltpunt of het stolpunt van water. Verschillende stoffen hebben een verschillend smeltpunt.
Als een vloeistof in een gas verandert, dan noemen we dit verdampen. Als een gas in een vloeistof verandert, dan noemen we dit condenseren (of condensatie). Water verdampt als we het verwarmen boven de 100 °C en condenseert als we het afkoelen onder de 100 °C. We noemen 100 °C daarom het kookpunt van water. Verschillende stoffen hebben een verschillend kookpunt. Condensatie treedt bijvoorbeeld op in de linker onderstaande afbeelding. Waterdamp in de lucht komt in aanraking met de koude fles en op deze manier ontstaan waterdruppeltjes aan de buitenkant van de fles. Ook dauw en mist ontstaan door condensatie (zie de twee rechter afbeeldingen).

Als een gas in een vaste stof verandert, dan noemen we dit rijpen. Als een vaste stof in een gas verandert, dan noemen we dit sublimeren. Als het in de winter vriest, dan kan de waterdamp uit de lucht direct bevriezen. Bij het rijpen van water ontstaan kleine ijskristalletjes (zie de onderstaande afbeeldingen). De ijskristallen in de vrieskist zijn ook door rijpen ontstaan. Sublimeren komt minder vaak voor. Tijdens droge winterdagen zien we soms sneeuw verdwijnen, terwijl het de hele dag heeft gevroren. Sneeuw is in dat geval gesublimeerd tot waterdamp.

Ook faseovergangen kunnen we met het deeltjesmodel beschrijven. Als we de vaste stof verwarmen, dan gaan de moleculen steeds harder trillen. Als het smeltpunt bereikt is, dan gaan de moleculen zo hard trillen, dat ze niet meer op hun vaste plek kunnen blijven zitten. Hoewel de moleculen nog steeds dicht tegen elkaar aan liggen, beginnen de moleculen nu langs elkaar te bewegen. Als dit gebeurt, is het materiaal aan het smelten en ontstaat er een vloeistof. Als we de stof nog verder verwarmen, dan bereiken we op een gegeven moment het kookpunt. Bij het kookpunt bewegen de moleculen zo snel dat ze ontsnappen uit de vloeistof. Als dit gebeurt, is het materiaal aan het verdampen en ontstaat er een gas.
|
|
|
1. Hoe noem je de faseovergang van een gas naar een vloeistof?
2. Hoe noem je de faseovergang van een vaste stof naar een gas?
3. Geef in de volgende situaties aan welke faseovergang er plaats vindt: a. Bij koud weer komen nevelwolkjes uit je mond. b. Een koud glas limonade beslaat aan de buitenkant. c. Er vormen zich ijskristallen op de producten in de vriezer. d. Kleren drogen snel op in de wind. e. Je maakt ijsklontjes in de vriezer. f. De badkamerspiegel beslaat als je de douche uit stapt. g. Mist klaart op in de loop van de ochtend. h. Er vormen zich dauwdruppels op grassprieten.
4. Leg uit waarom een faseovergang geen chemische reactie is.
5. Leg met het deeltjesmodel uit dat gas wel gemakkelijk samengeperst kan worden en een vloeistof niet.
6. Leg met het deeltjesmodel uit dat je sommige kristallen in sommige richtingen vrij gemakkelijk kan splijten en in andere richtingen niet.
7. Is het vast worden van het ei een faseovergang of niet?
8. Een leerling komt een kamer binnen en zijn bril beslaat. Leg uit wat er gebeurd is en onder welke omstandigheden dit gebeurt.
9. Zoek het smeltpunt van de volgende stoffen op en leg telkens uit of de stof vast is bij kamertemperatuur (20 °C): aceton, glucose en methaan.
10. Eenzelfde plas water kan op een bepaalde dag veel meer tijd nodig hebben om te verdampen dan op een andere dag. Geef hiervoor een verklaring.
11. De lucht bevat maximaal 4% waterdamp. Bij het condenseren van deze waterdamp ontstaat bijvoorbeeld mist. De lucht bevat ook 80% stikstof. Leg uit waarom stikstofgas niet condenseert en waterdamp wel.
12. Leg met behulp van het deeltjesmodel uit wat er gebeurt als een vloeistof verdampt.
13. In de volgende afbeelding zien we bij A stoom ontsnappen uit een ketel. Bij B wordt de stoom een nevel. Uiteindelijk lijkt de nevel 'in het niets' te verdwijnen. Geef bij elk van deze drie processen de naam van de faseovergang.
14. Wat bevindt zich tussen de deeltjes in de gasfase?
15. Vloeibare stikstof gaat koken bij kamertemperatuur. Leg uit waarom dit gebeurt.
16. Als we een opgeblazen ballon onderdompelen in vloeibare stikstof, dan krimpt de ballon. Verklaar dit met het deeltjesmodel.
17. Ether is een vloeistof die erg snel verdampt. De snelste deeltjes in ether zijn bij kamertemperatuur al snel genoeg om uit de vloeistof te ontsnappen. Verklaar met het deeltjesmodel wat er met de temperatuur van ether gebeurt als de snelste deeltjes ontsnappen.
|
§3 Warmtetransport
In deze paragraaf gaan we het hebben over het verschil tussen warmte en temperatuur en gaan we drie manieren bestuderen waarop warmte kan stromen van de ene plek naar de andere.
Stel je legt een stuk ijzer met een temperatuur van 60 °C tegen een even groot stuk ijzer met een temperatuur van 0 °C (zie de onderstaande afbeelding). Door de hogere temperatuur trillen de deeltjes in het linker blok sneller. Deze snel trillende deeltjes in het linker blok botsen tegen de minder snelle deeltjes in het rechter blok. Als gevolg hiervan remmen de deeltjes in het linker blok wat af en gaan de deeltjes in het rechter blok juist sneller trillen. De temperatuur van het linker blok neemt hierdoor af en de temperatuur in het rechter blok neemt hierdoor toe. Dit proces gaat door totdat de deeltjes in beide stukken evenveel trillen. Dit gebeurt als de temperatuur gelijk wordt. Als er geen warmte verloren gaat aan de omgeving en als de blokken even groot zijn, dan zal de temperatuur van beide blokken uiteindelijk 30 °C worden.

Hoe harder de deeltjes in een stof trillen, hoe meer energie deze deeltjes hebben. In het hierboven beschreven proces is dus energie verplaatst van het linker naar het rechter blok. Het soort energie dat hier verplaatst is noemen we de warmte (Q). De SI-eenheid van de energie is joule (J). Ook de warmte heeft dus als SI-eenheid de joule.
Het is belangrijk om onderscheid te maken tussen warmte en temperatuur. De temperatuur is datgene dat we met een thermometer meten en de eenheid hiervan is graden Celsius of kelvin. Warmte is een soort energie en de eenheid hiervan is de joule. Er geldt dus:
|
Temperatuur (T) |
kelvin (K) |
|
Energie (J) |
joule (J) |
|
Warmte (Q) |
joule (J) |
We hebben gezien dat in het bovenstaande voorbeeld een deel van de energie in het linker blok overgedragen is naar het rechter blok. We hebben daarom geconcludeerd dat er warmte is verplaatst van links naar rechts. In het dagelijks leven zeggen we ook wel dat 'kou' zich verplaatst van rechts naar links. Het linker blok is immers kouder geworden. In de natuurkunde wordt deze manier van denken echter zo veel mogelijk vermeden. De energie stroomt immers van hoge naar lage temperatuur en niet andersom. Een zin als 'doe het raam dicht, want er komt kou binnen' is natuurkundig gezien dus onhandig.
Hoeveel warmte er zal stromen van een plek met hoge temperatuur naar een plek met lage temperatuur hangt af van het temperatuurverschil (ΔT) tussen deze twee plekken. Hoe groter het temperatuurverschil, hoe meer warmte er zal stromen. Als gevolg neemt de temperatuur van het warme voorwerp sneller af en van het koude voorwerp sneller toe.
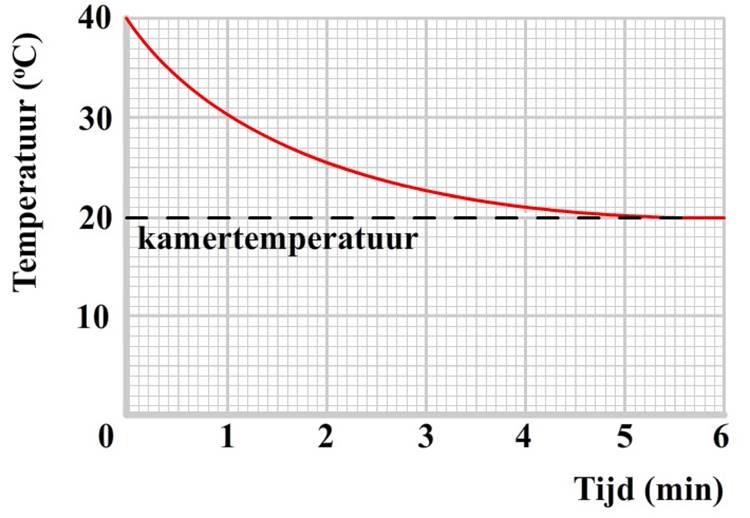
We kunnen dit goed zien in het onderstaande diagram. Het diagram geeft het afkoelen van een klein voorwerp in een kamer met een temperatuur van 20 graden Celsius weer. Merk op dat bij een groter temperatuurverschil, de snelheid van het voorwerp sneller afneemt. De warmte die het voorwerp uitstroomt, komt in de kamer terecht. Omdat een kamer redelijk groot is, zal de kamer hierdoor niet significant opwarmen.
Het stromen van warmte noemen we ook wel warmtetransport. Er bestaan drie soorten warmtetransport:
· Warmtegeleiding
· Warmtestroming
· Straling
 Warmtegeleiding
(ook wel gewoon geleiding genoemd) ontstaat doordat atomen hun warmte doorgeven
doordat ze tegen elkaar botsen. Stel dat een stuk metaal op één plek
wordt verwarmd. Als gevolg gaan op deze plek de deeltjes sneller trillen. Deze
deeltjes botsen dan tegen de omringende deeltjes en deze worden als gevolg ook
in trilling gebracht. Op deze manier trekt de warmte door het materiaal. We
zien dit effect bijvoorbeeld als we een metalen lepel in een pan kokend water
plaatsen. De warmte trekt dan door het metaal omhoog (zie de rechter
afbeelding).
Warmtegeleiding
(ook wel gewoon geleiding genoemd) ontstaat doordat atomen hun warmte doorgeven
doordat ze tegen elkaar botsen. Stel dat een stuk metaal op één plek
wordt verwarmd. Als gevolg gaan op deze plek de deeltjes sneller trillen. Deze
deeltjes botsen dan tegen de omringende deeltjes en deze worden als gevolg ook
in trilling gebracht. Op deze manier trekt de warmte door het materiaal. We
zien dit effect bijvoorbeeld als we een metalen lepel in een pan kokend water
plaatsen. De warmte trekt dan door het metaal omhoog (zie de rechter
afbeelding).
Niet alle stoffen geleiden warmte even goed. Een metalen lepel in een pan met kokend water wordt bijvoorbeeld veel sneller warm dan een houten lepel. Metaal wordt daarom een goede geleider genoemd en hout een slechte geleider. Slechte geleiders worden ook wel isolatoren genoemd.
Ook gassen en vloeistoffen zijn isolatoren. Dat bijvoorbeeld lucht een goede isolator is kan je goed ervaren door je hand dicht naast een vlam te houden (zie de onderstaande afbeelding). Je hand zal hierdoor niet erg opwarmen. Als je je hand boven de kaars houdt, dan voel je wel snel de warmte. Dit komt echter door een ander effect, genaamd warmtestroming, dat de later in deze paragraaf zullen bespreken.

Een thermosfles maakt goed gebruik van deze eigenschap van lucht. Een thermosfles bestaat uit twee flessen met daartussen lucht en als gevolg stroomt warmte lastig de fles in en lastig de fles uit. Warme dranken blijven hierdoor langer warm en koude dranken langer koud. Hetzelfde principe wordt toegepast bij dubbelglas. Dubbelglas bestaat uit twee glazen met daartussen lucht. Dit zorgt ervoor dat we weinig warmte verliezen via de ramen.
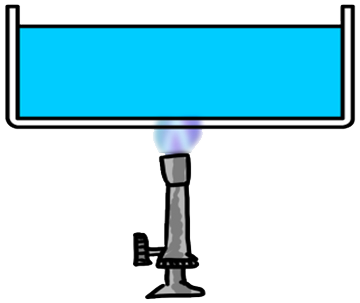
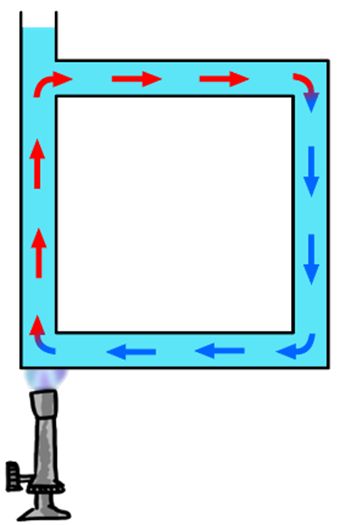
Hoewel gassen en vloeistoffen geen goede geleiders zijn, kan warmte hierin wel goed worden getransporteerd met behulp van warmtestroming. We kunnen dit effect goed zien in de onderstaande linker afbeelding. Door geleiding zal alleen het water in de buurt van de vlam opwarmen. Dit warme water zet uit en als gevolg wordt de dichtheid van het water kleiner en zal het opstijgen. Als gevolg begint het water rond te stromen.
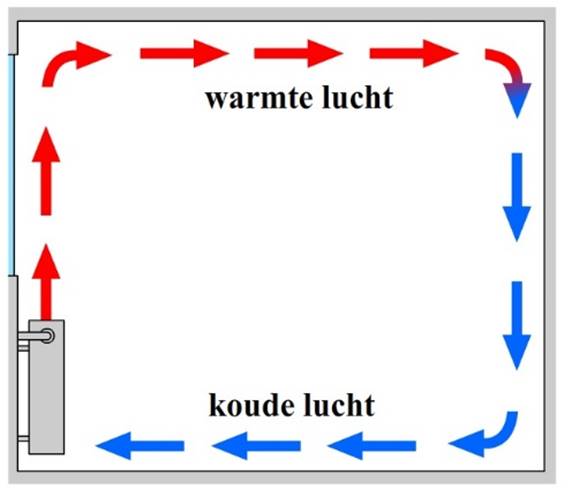
Ook het verwarmen van een kamer gebeurt via warmtestroming (zie de onderstaande afbeelding). De verwarming zelf kan met behulp van geleiding alleen de lucht verwarmen die direct in contact staat met de verwarming. Deze lucht wordt hierdoor warmer, krijgt een lagere dichtheid en stijgt op. Als gevolg ontstaat er een warmtestroom in de kamer en wordt de kamer steeds warmer.
 De
derde soort warmtetransport wordt straling genoemd. Een ander woord voor
straling is licht. Dat straling warmte kan overdragen weten we als we
onze handen in de zon houden. Als het zonlicht door onze huid wordt
geabsorbeerd, wordt onze huid warmer. Hetzelfde effect treedt ook op als je je
handen warmt aan een kampvuur of openhaard. Er is ook straling die we niet met
onze ogen kunnen zien. Wijzelf zenden bijvoorbeeld infraroodstraling
uit. In de rechter afbeelding is een foto gemaakt met een infraroodcamera.
Zoals je ziet geeft warm water ook infrarood licht af. Je kunt deze
infraroodstraling bijvoorbeeld voelen als je je hand naast een hete verwarming
plaatst (boven de verwarming heeft warmtestroming de overhand).
De
derde soort warmtetransport wordt straling genoemd. Een ander woord voor
straling is licht. Dat straling warmte kan overdragen weten we als we
onze handen in de zon houden. Als het zonlicht door onze huid wordt
geabsorbeerd, wordt onze huid warmer. Hetzelfde effect treedt ook op als je je
handen warmt aan een kampvuur of openhaard. Er is ook straling die we niet met
onze ogen kunnen zien. Wijzelf zenden bijvoorbeeld infraroodstraling
uit. In de rechter afbeelding is een foto gemaakt met een infraroodcamera.
Zoals je ziet geeft warm water ook infrarood licht af. Je kunt deze
infraroodstraling bijvoorbeeld voelen als je je hand naast een hete verwarming
plaatst (boven de verwarming heeft warmtestroming de overhand).
|
|
|
1. Geef de SI-eenheid van warmte en van temperatuur.
2. Als we onze handen in de sneeuw leggen, dan voelt het alsof de 'kou' in onze handen trekt. Leg uit waarom deze uitspraak niet correct is.
3. Een koekenpan is meestal gemaakt van metaal, maar de handvaten zijn meestal gemaakt van kunststof. Leg uit waarom deze materialen gebruikt worden.
4. Wat is het nadeel van metalen eetborden?
5. Dubbele beglazing bestaat uit twee ruiten met daartussen een laagje lucht. Wat is het voordeel hiervan?
6. Waarom staat de vloer van een kinderbox altijd een stukje van de grond af?
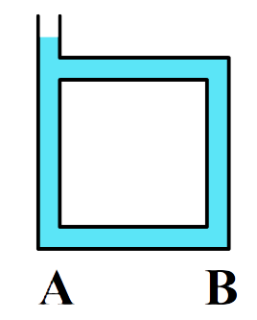
7. Bestudeer de onderstaande afbeelding. a. Hoe gaat de vloeistof stromen als je de buis verwarmt bij punt A? b. Hoe gaat de vloeistof stromen als je de buis verwarmt bij punt B? 8. Teken de warmtestroming in deze bak met water:
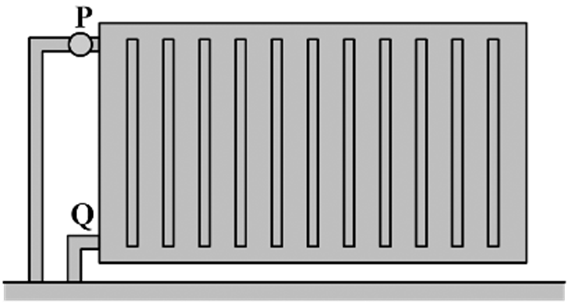
9. Hieronder is een verwarming getekend. Leg uit of de verwarming van P naar Q of van Q naar P moet stromen om de verwarming optimaal te laten werken.
10. In een thermosfles kunnen vloeistoffen lang koud en lang warm worden gehouden. Dit gebeurt doordat het warmtetransport van binnen naar buiten geminimaliseerd wordt. De thermosfles bestaat uit een dubbele wand met daartussen een laagje lucht. Aan de binnenkant van de fles is ook een glanzend oppervlak aangebracht. a. Leg uit waarom de thermosfles zo goed werkt. b. Bij een duurdere variant wordt de lucht tussen de twee wanden ook nog weggepompt. We spreken dan van een vacuümthermosfles. Wat is het voordeel van deze fles?
11. Een verwarming verwarmt een kamer. Welke soorten warmtetransport zorgen hier voor het verwarmen van de kamer en welke (bijna) niet? Leg je antwoord uit.
12. Als je je hand 5 centimeter naast een brandende kaars houdt, dan voel je amper de warmte. Als je je hand 5 cm boven de brandende kaars houdt, dan voel je de warmte heel sterk. Wat zorgt voor dit verschil?
|