Hoofdstuk 3
Scheidingsmethoden
§1 Stofeigenschappen
§2 Bezinken en filtreren
§3 Indampen en destilleren
§4 Extraheren en adsorptie
§5 Water zuiveren
§1 Stofeigenschappen
In dit hoofdstuk bespreken we een aantal methodes om mengsels te scheiden. Dit kunnen we doen door gebruik te maken van de verschillende stofeigenschappen van stoffen. Wat stofeigenschappen zijn bespreken we in deze paragraaf.
Sommige eigenschappen van stoffen kunnen gebruikt worden om de stoffen te herkennen. We noemen dit stofeigenschappen. Een stuk goud heeft bijvoorbeeld altijd deze eigenschappen:
- Gele kleur
- Glanzend
- Vast bij kamertemperatuur
- Vervormbaar
- Goede geleider van elektriciteit
- Niet brandbaar
- Smeltpunt van 1064 graden Celsius
- Kookpunt van 2856 graden Celsius
- Dichtheid van 19,3 g/cm3
Als we een stof vinden met al deze eigenschappen, dan weten we dat dit goud is. Als het één van deze eigenschappen niet heeft, dan weten we zeker dat het geen goud is.
Niet alle eigenschappen van een stof zijn ook meteen stofeigenschappen. Als je een stuk goud hebt met een massa van 500 gram dan wil dat niet zeggen dat elk stuk goud een massa van 500 gram heeft. Massa is dus geen stofeigenschap. De dichtheid van goud is wel een stofeigenschap, want de dichtheid van elk stuk goud is 19,3 g/cm3.
Ook de fase van een stof is geen stofeigenschap. Goud kan voorkomen als vaste stof, maar ook als vloeistof of gas. De fase bij kamertemperatuur is wel een stofeigenschap. Goud is bij kamertemperatuur immers altijd een vaste stof.
 Leerdoelen:
Leerdoelen:
|
- Zorg dat je kan beredeneren of iets een stofeigenschap is of niet.
- Zorg dat je begrijpt dat de fase van een stof en de massa geen stofeigenschappen zijn, maar de fase bij kamertemperatuur en de dichtheid wel.
|
 Opdrachten
Opdrachten
|
-
(6p) Geef bij elk van de volgende eigenschappen aan of het gaat om stofeigenschappen:
- de fase
- de fase bij kamertemperatuur
- de kleur
- de massa
- de brandbaarheid
- de temperatuur
- de dichtheid
-
Noem telkens een stofeigenschap die de volgende stoffen gemeen hebben
en een stofeigenschap die ze niet gemeen hebben:
- (2p) Water en alcohol
- (2p) Suiker en keukenzout
- (2p) Koper en ijzer
-
(3p) Een persoon vindt een blokje van een onbekend materiaal en noteert de volgende eigenschappen. Het staafje glimt, heeft de vorm van een kubus, is vast bij kamertemperatuur en geleid warmte goed. Welke van deze eigenschappen zijn stofeigenschappen?
-
Een leerling vindt een oude munt en wilt weten of deze van puur zilver gemaakt is. De leerling ziet dat de munt een ronde vorm heeft, een grijze kleur heeft en vast is bij kamertemperatuur. Ook heeft de munt een dichtheid van 8,0 g/cm3.
- (3p) Welk van deze eigenschappen zijn stofeigenschappen.
- (2p) Leg uit of de munt van puur zilver gemaakt kan zijn.
-
Een leerling vindt een onbekend poeder in de keuken. De dichtheid is 1,58 g/cm3, de massa is 155 gram, de stof is wit van kleur, de stof smelt bij 185 graden Celsius, de stof zit in een kartonnen doos en de stof is oplosbaar in water.
- (2p) Welk van deze eigenschappen zijn geen stofeigenschappen? Leg je antwoord uit.
- (3p) Ga met BINAS na om welke stof het hier gaat. Geef drie waarnemingen die hiermee overeenstemmen.
|
§2 Bezinken en filtreren
In deze paragraaf beginnen we met het bespreken van scheidingsmethoden. Dit zijn methoden waarmee we de stoffen in een mengsel kunnen scheiden. We beginnen met bezinken en filtreren.
Het is gemakkelijk om van twee zuivere stoffen een mengsel te maken, maar het omgekeerde is vaak lastiger. Stel je mengt suiker en meel. In dat geval komen vele duizenden suikerkorrels en meelkorrels door elkaar te liggen. Het lijkt misschien een onmogelijke taak om deze stoffen weer te scheiden, maar toch bestaan er een aantal technieken om dit te doen. We noemen dit scheidingsmethoden.
Scheidingsmethoden maken gebruik van verschillende stofeigenschappen van de gemengde stoffen. In de rest van het hoofdstuk gaan we hier voorbeelden van zien.
De simpelste scheidingsmethode wordt bezinken genoemd. Stel we hebben een mengsel van zand en water. Om dit mengsel voor een deel te scheiden hebben we alleen een beetje geduld nodig. Omdat zand een grotere dichtheid heeft dan water, zakt het na verloop van tijd vanzelf naar de bodem (zie de onderstaande afbeelding). De stof die op de bodem komt te liggen—in dit geval het zand—noemen we het bezinksel. Het water kan je daarna voorzichtig afgieten. Deze scheidingsmethode maakt dus gebruik van het verschil in de stofeigenschap dichtheid.

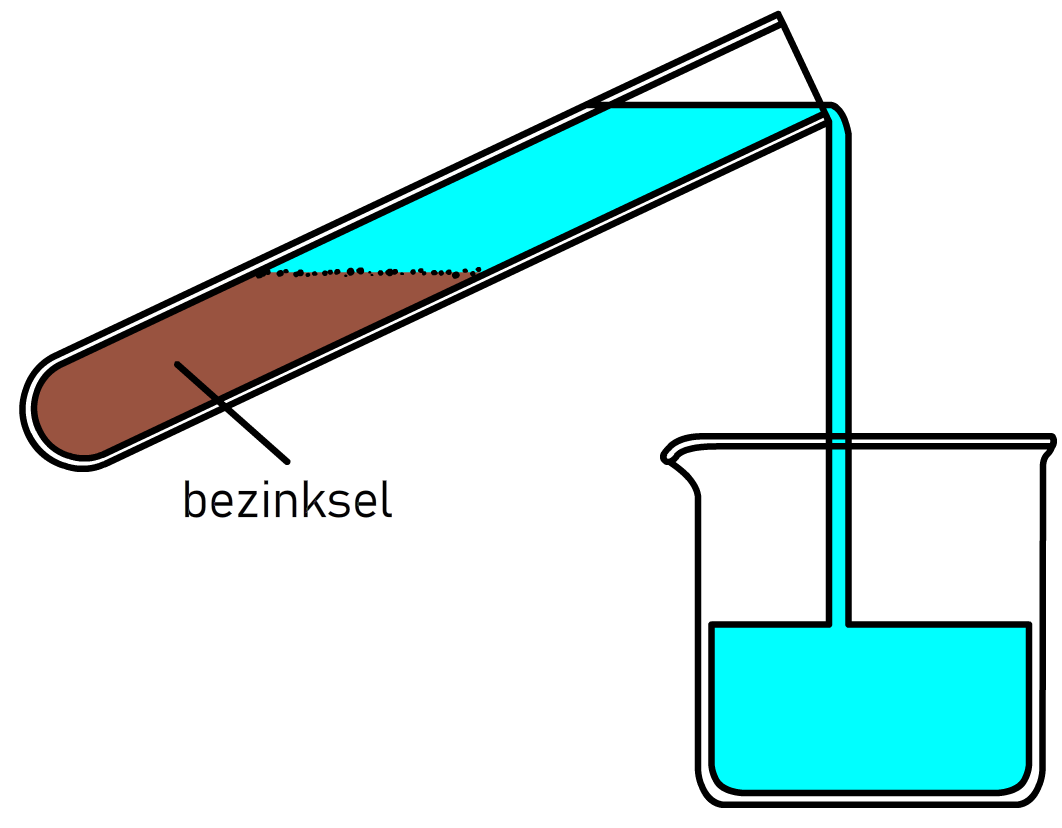 (Afbeelding: Tummers77; CC BY-SA 4.0)
(Afbeelding: Tummers77; CC BY-SA 4.0)
Een andere bekende scheidingsmethode wordt filtreren genoemd. Hiermee kunnen we suspensies scheiden. Een filter is een stukje papier met daarin microscopische gaatjes waar losse deeltjes gemakkelijk doorheen gaan, maar waar de klontjes in een suspensie in blijven steken. In de onderstaande afbeelding zien we een gele suspensie die in een filter wordt geschonken. De gele korrels blijven in het filter hangen, terwijl de waterdeeltjes gemakkelijk door het filter stromen en in het bekerglas terecht komen. De stof die achterblijft in het filter noemen we het residu (in dit geval de gele korrels). De stof die door het filter stroomt noemen we het filtraat (in dit geval water).
Bij deze scheidingsmethode wordt dus gebruik gemaakt van de stofeigenschap deeltjesgrootte om de stoffen te kunnen scheiden.

Stel dat we een mengsel van meel, water en zout filtreren, dan blijven de grote meelklontjes in het filter steken. Dit vormt dus het residu. De water- en de zoutdeeltjes zijn wel klein genoeg om door het filter te gaan en vormen het filtraat.
Een mondkapje is ook een voorbeeld van een filter. Lucht gaat moeiteloos door dit filter heen, omdat dit gas uit losse deeltjes bestaat. Rookdeeltjes blijven bijvoorbeeld in het filter hangen, omdat deze stoffen uit grotere klontjes vaste stof bestaan. Op deze manier kunnen we ademen zonder deze rookdeeltjes binnen te krijgen. Het nadeel van een mondkapje is dat schadelijke gassen wel gewoon door het filter heen gaan. Hiertegen beschermt een mondkapje dus niet.
 Leerdoelen:
Leerdoelen:
|
- Zorg dat je weet dat je sommige mengsels kan scheiden door middel van bezinken. Doordat stoffen verschillen in de stofeigenschap dichtheid, zakken sommige stoffen naar de bodem. We noemen dit het bezinksel.
- Zorg dat je weet dat je o.a. suspensies kan scheiden door middel van filtratie. Doordat stoffen verschillen in de stofeigenschap deeltjesgrootte, blijven sommige stoffen in het filter steken, terwijl andere stoffen door het filter heen gaan.
- Zorg dat je kan achterhalen wat het filtraat en wat het residu is bij een filtratie en zorg dat je kan uitleggen dat oplossingen en gassen door een filter heen gaan.
|
 Opdrachten
Opdrachten
|
-
Als je een pot verf lang laat staan, dan zakt het pigment (dat de verf kleur geeft) naar beneden, terwijl daarboven een oplosmiddel zichtbaar blijft (waardoor de verf vloeibaar blijft).
- (1p) Welke scheidingsmethode heeft hier plaatsgevonden?
- (1p) Welk verschil in stofeigenschap is bij deze scheidingsmethode gebruikt?
-
Leg uit of je de volgende mengsels kan scheiden met filtratie. Benoem ook telkens wat het residu is en wat het filtraat.
- (2p) Een mengsel van suiker en water
- (2p) Een mengsel van meel en water
- (2p) Een mengsel van limonadesiroop en water
- (2p) Een mengsel van suiker en meel (je mag water toevoegen)
- (2p) Een mengsel van zout en suiker (je mag water toevoegen).
-
(2p) In een bekerglas met een flinke hoeveelheid water doet men een beetje zout, krijt en zand. Het geheel wordt goed geroerd en gefiltreerd. Leg uit waaruit het filtraat en waaruit het residu bestaat.
-
Een leerling bevindt zich in een bevuilde stad en besluit een mondkapje te dragen.
- (2p) Leg uit of een mondkapje werkt tegen giftige gassen.
- (2p) Leg uit of een mondkapje werkt tegen rook.
- (2p) Wat is bij het ademen door een mondkapje in een omgeving met rook het residu en wat is het filtraat.
-
(1p) Bij filtreren wordt gebruikgemaakt van een verschil in een stofeigenschap. Welke stofeigenschap is dit?
-
(2p) Opgeloste ijzerdeeltjes worden uit water verwijderd door dit water in aanraking te laten komen met zuurstof in de lucht. Als gevolg ontstaan kleine vaste stukjes ijzeroxide. IJzeroxide heeft een grotere dichtheid dan water. Welke twee scheidingsmethoden liggen het meest voor de hand om het ijzer te scheiden van het water.
-
(2p) In landen met veel plastic afval worden geregeld barrières in het wateroppervlak geplaatst om dit plastic op te vangen, zodat het daarna efficiënt opgeruimd kan worden (zie de onderstaande foto). Wat is in dit geval het filtraat en het residu?

-
In hoogovens wordt ijzer verkregen door het te laten reageren met koolstof en zuurstof. Het ijzer dat ontstaat smelt en zakt naar de bodem waar het afgetapt kan worden.
- (1p) Welke scheidingsmethode is hier gebruikt.
- (1p) Welk verschil in stofeigenschap wordt bij deze scheidingsmethode gebruikt?
|
§3 Indampen en destilleren
In deze paragraaf gaan we nog twee scheidingsmethoden bestuderen genaamd indampen en destilleren.
In de vorige paragraaf hebben we geleerd dat we suspensies kunnen scheiden met een filter. In het geval van een oplossing gaat dit echter niet lukken. Een oplossing bestaat immers uit allemaal losse deeltjes en die gaan dus allemaal door het filter. We hebben in dat geval dus een andere scheidingsmethode nodig.
De simpelste manier om een oplossing te scheiden wordt indampen genoemd. Indampen is het verhitten van een oplossing, zodat één stof in de oplossing verdampt, terwijl de andere achterblijft (zie de onderstaande afbeelding). Neem bijvoorbeeld zeewater. Als we zeewater aan de kook brengen, dan zal het water verdampen, maar het zout niet. Zout heeft namelijk een kookpunt van wel 1413 °C, terwijl het kookpunt van zeewater net iets boven de 100 °C ligt. Bij deze techniek maken we dus gebruik van het verschil in de stofeigenschap kookpunt om verschillende stoffen te scheiden.
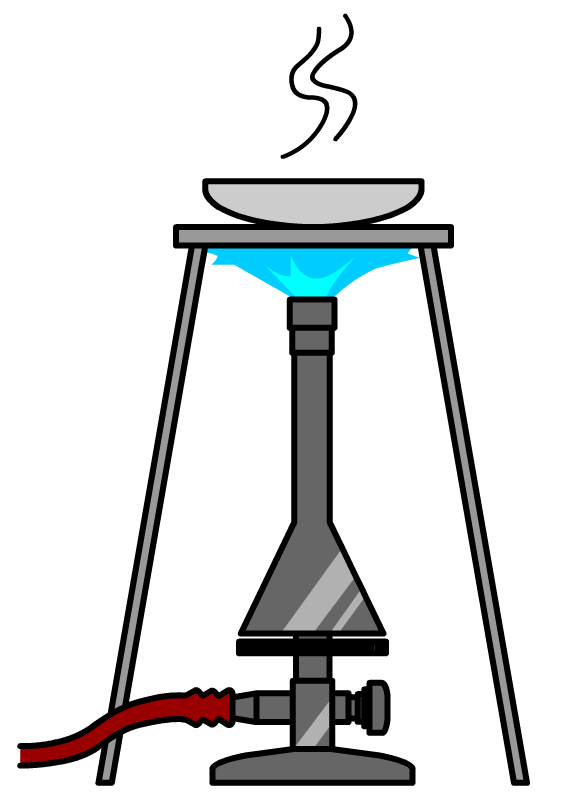
Bij indampen van zeewater hou je zout over, maar wat als je nu juist het water wilt hebben, bijvoorbeeld om drinkwater van zeewater te maken? In dat geval gebruiken we een scheidingsmethode die destillatie wordt genoemd. Bij destillatie vangen we de verdampte stof op in een afgekoelde buis. De lage temperatuur van deze buis zorgt ervoor dat de verdampte stof gemakkelijk condenseert. De druppels die hierbij ontstaan, glijden door de buis naar beneden en worden opgevangen in een erlenmeyer (zie de onderstaande afbeelding). De stof die achterblijft noemen we wederom het residu. De stof die opgevangen wordt noemen we het destillaat.
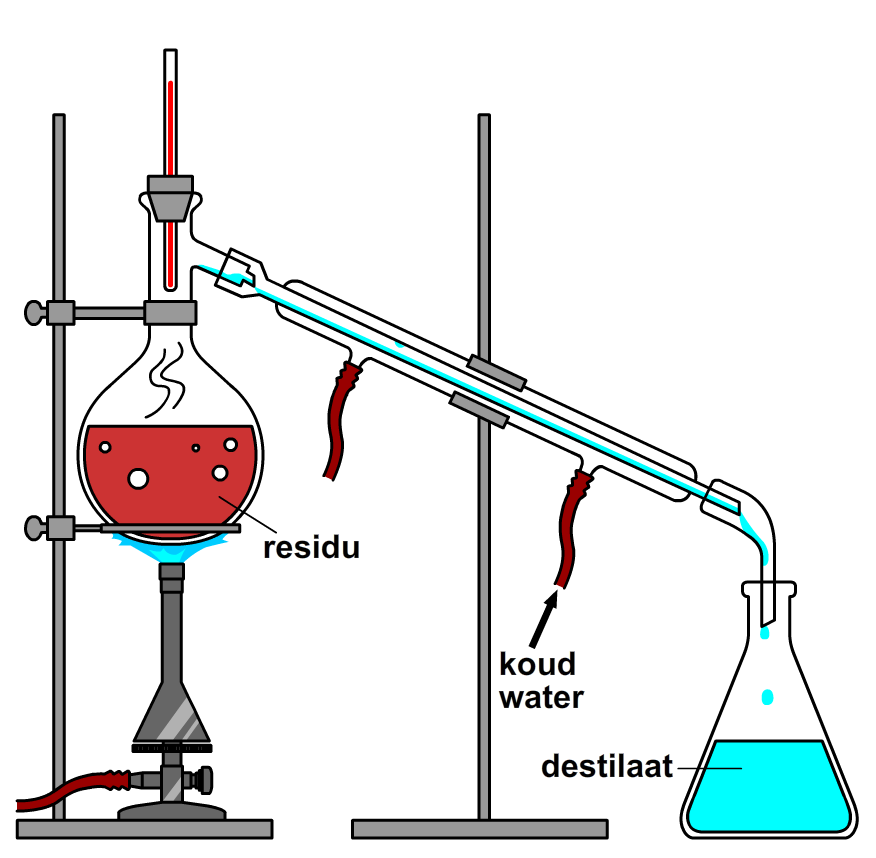
 EXPERIMENT
EXPERIMENT
|
|
In de rechter video zie je de destillatie van wijn. De alcohol verdampt en condenseert daarna en komt terecht in een erlenmeyer.
|
 DEMO-VIDEO:
Destillatie van wijn
DEMO-VIDEO:
Destillatie van wijn
|
|
Destillatie kan bijvoorbeeld gebruikt worden om (bijna) zuivere alcohol uit wijn te halen. Wijn bestaat voor het grootste gedeelte uit water en alcohol. Water heeft een kookpunt van 100 °C en alcohol van 78 °C. Als we de wijn verhitten tussen deze twee kookpunten in, dan verdampt de alcohol wel, maar het water niet. Op deze manier kan
je bijna pure alcohol verkrijgen. Pure alcohol is een brandstof en kan met een lucifer in brand worden gestoken (zie de onderstaande afbeelding).
 (Afbeelding: SirVir; CC BY-SA 3.0)
(Afbeelding: SirVir; CC BY-SA 3.0)
Ook als we kraanwater indampen of destilleren blijft er een residu achter. We noemen dit kalk (zie de onderstaande afbeelding). Ditzelfde proces zorgt bijvoorbeeld voor kalkaanslag in de badkamer. Het water dat we opvangen bij de destillatie van water noemen we gedestilleerd water. Dit is (bijna) zuiver water.

 Leerdoelen:
Leerdoelen:
|
- Zorg dat je weet dat je oplossingen kan scheiden door middel van indampen en destillatie. Doordat stoffen verschillen in de stofeigenschap kookpunt, kunnen sommige stoffen verdampen, terwijl andere stoffen achterblijven als vloeistof.
- Zorg dat je begrijpt dat de temperatuur van het mengsel bij indampen en destilleren tussen de kookpunten van de stoffen in moet zitten.
- Zorg dat je onderscheid kunt maken tussen het destillaat en het residu bij een destillatie.
|
 Opdrachten
Opdrachten
|
- (1p) Noem de scheidingsmethode waarmee je zout kan winnen uit zeewater.
- (1p) Noem de scheidingsmethode waarmee je zuivere alcohol kan winnen uit wijn.
-
(2p) Welke twee faseovergangen vinden bij destillatie plaats?
-
(2p) Leg uit wat het verschil is tussen kraanwater en gedestilleerd water.
- (1p) Is indampen geschikt voor het verkrijgen van zuiver water uit zeewater? Leg je antwoord uit.
-
Een mengsel van aceton en alcohol wordt gedestilleerd.
- (1p) Tot welke temperatuur moet je het mengsel hiervoor verwarmen? (Maak hier gebruik van BINAS)
- (1p) Welke stof wordt het destillaat en welke het residu?
-
Lucht is een mengsel van vooral zuurstof en stikstof.
- (1p) Deze gassen hebben een verschillend kookpunt. Leg uit hoe je deze twee stoffen kunt scheiden.
- (2p) Noem een temperatuur die hiervoor geschikt is.
-
(2p) De waterkringloop beschrijft de cyclus waarbij water uit de zee verdampt, als regen neervalt op land en via rivieren weer terugstroomt naar de zee. Leg uit waarom (een deel) van dit proces met destillatie vergeleken wordt.
-
(2p) De Dode Zee heeft een extreem hoog zoutgehalte. Leg uit hoe dit zou kunnen komen en vertel op welke scheidingsmethode dit proces het meest lijkt.
|
§4 Extractie en adsorptie
In deze paragraaf gaan we nog twee scheidingsmethoden bestuderen, genaamd extractie en adsorptie.
Een andere scheidingsmethode wordt extraheren of extractie genoemd. Extraheren werkt als één van de stoffen in een mengsel oplosbaar is en de andere niet. Hier scheiden we dus op basis van de stofeigenschap oplosbaarheid. In zoutmijnen zit zout bijvoorbeeld vaak vast in poreuze stenen. Als we het zout uit de stenen willen verwijderen, dan voegen we eerst warm water toe. Het zout lost op in dit water, maar het steen natuurlijk niet. Het opgeloste zout kan dan opgepompt worden. Door middel van indampen kan het zout dan gewonnen worden.
We zijn ook aan het extraheren als we een theezakje in heet water dopen. Een aantal stoffen uit de theeblaadjes lost op in het water, terwijl de blaadjes zelf niet oplossen (zie de onderstaande linker afbeelding). Merk op dat het theezakje ook dient als een filter, waar de theeblaadjes niet doorheen kunnen.
In de rechter afbeelding zien we een theezakje in koud water en een theezakje in warm water. Zoals je kan zien werkt extraheren beter bij hogere temperatuur. Dit komt omdat deeltjes bij hogere temperatuur sneller bewegen en hierdoor lossen stoffen sneller op.

 (Afbeelding: Pixabay; PD)
(Afbeelding: Pixabay; PD)
Een andere scheidingsmethode wordt adsorptie genoemd (niet te verwarren met 'absorptie'). Adsorptie is het proces waarbij moleculen zich hechten
aan een andere stof. Hoe goed stoffen hechten aan andere stoffen is ook een stofeigenschap. Het bekendste adsorptiemiddel is actieve kool. Dit is een zwart poeder waarin vele microscopische poriën zitten (zie de onderstaande afbeeldingen).

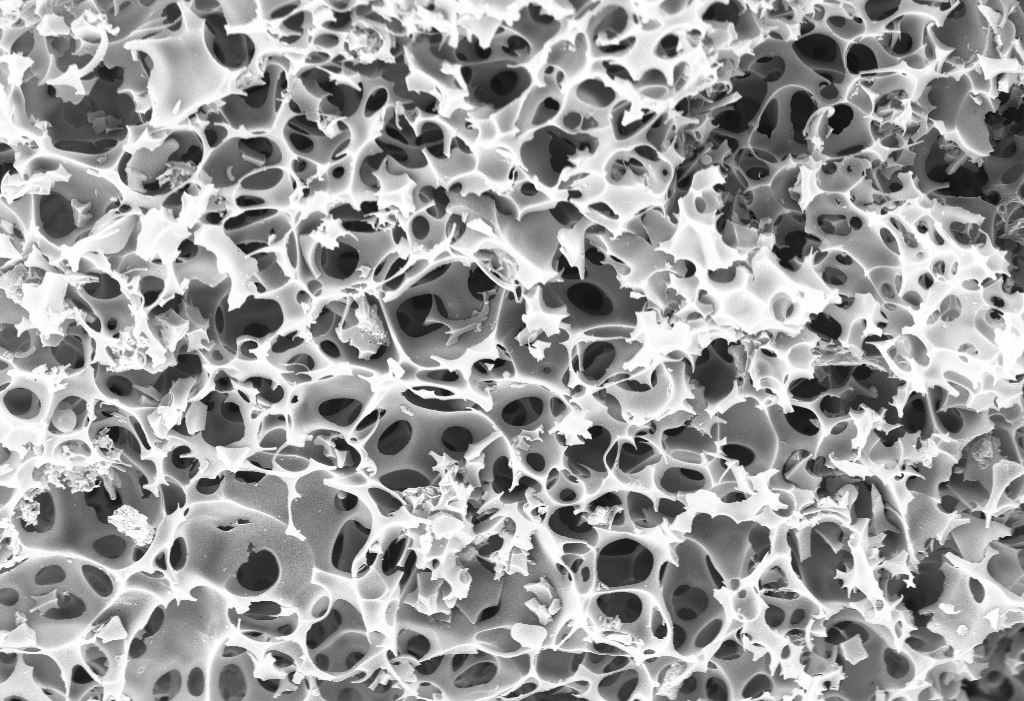 (Afbeelding: Ravedave; CC BY 2.5 / SomnathWiki007; CC BY 4.0)
(Afbeelding: Ravedave; CC BY 2.5 / SomnathWiki007; CC BY 4.0)
Sommige stoffen blijven in deze poriën vastzitten. Actieve kool wordt bijvoorbeeld gebruikt om kleurstoffen te verwijderen uit vloeistoffen. Als we van slootwater drinkwater willen maken, dan kunnen we actieve kool bijvoorbeeld gebruiken om de gelige kleur van het slootwater te verwijderen (zie de onderstaande linker afbeeldingen). Ook wordt actieve kool gebruikt in gasmaskers om gevaarlijke gassen uit de lucht te filteren (zie de rechter afbeelding).


 EXPERIMENT
EXPERIMENT
|
In de onderstaande video's zien we dat actieve kool de blauwe kleurstof methyleenblauw verwijdert uit een vloeistof en NO2 verwijdert uit de lucht.
 DEMO-VIDEO:
Adsorptie van een vloeistof
DEMO-VIDEO:
Adsorptie van een vloeistof
 DEMO-VIDEO:
Adsorptie van een gas
DEMO-VIDEO:
Adsorptie van een gas
|
 Leerdoelen:
Leerdoelen:
|
- Zorg dat je weet dat je sommige mengsels kan scheiden door middel van extractie. Doordat stoffen verschillen in de stofeigenschap oplosbaarheid, lossen sommige stoffen op in een vloeistof, terwijl andere stoffen hun vaste vorm houden.
- Zorg dat je weet dat je sommige mengsels kan scheiden door middel van adsorptie. Doordat stoffen verschillen in de stofeigenschap hechtingsvermogen, komen sommige stoffen vast te zitten en andere stoffen niet.
- Zorg dat je weet dat je met actieve kool bijvoorbeeld kleurstoffen kan verwijderen uit een oplossing en ook sommige schadelijke gassen in de lucht.
|
 Opdrachten
Opdrachten
|
- (1p) Noem een voorbeeld waarbij extractie gebruikt wordt als scheidingsmethode.
- (1p) Noem een voorbeeld waarbij adsorptie gebruikt wordt als scheidingsmethode.
-
In sommige plekken in Nederland vinden we onder de grond
poreus steen dat gevuld is met zout. Om dit zout te verkrijgen pompen we water naar deze stenen, zodat het zout erin oplost.
- (1p) Welke scheidingsmethode is hier gebruikt?
- (1p) Wat moeten we daarna doen om het zout van deze oplossing te scheiden?
-
(4p) Welke twee scheidingsmethoden pas je toe als je een
theezakje in een kop thee doet? Geef in beide gevallen ook aan welke verschillen in stofeigenschappen voor het scheiden gebruikt zijn.
-
Bij bereiding van suiker uit suikerbieten worden de suikerbieten eerst in fijne reepjes gesneden. Vervolgens worden ze in een bak met heet water gedaan.
- (1p) Waarom worden de bieten eerst fijngesneden?
- (1p) Daarna worden de suikerbieten in heet water gedaan. Welke scheidingsmethode wordt hier toegepast?
- (2p) Noem een voordeel van het gebruik van heet water?
- (1p) Hoe kun je de suiker daarna uit de oplossing verkrijgen?
-
We kunnen bruine suiker wit maken door het op te lossen en een stof toe te voegen.
- (1p) Welke stof wordt hiervoor toegevoegd?
- (1p) Daarna moet deze stof weer gescheiden worden van de suikeroplossing. Welke scheidingsmethode hebben we hiervoor nodig?
- (1p) Daarna wil je het suiker uit de oplossing halen. Welke scheidingsmethode hebben we hiervoor nodig?
- (3p) Geef bij alle drie de scheidingsmethode aan welke verschillen in stofeigenschappen voor het scheiden gebruikt zijn.
In sommige steden in Azië lopen mensen geregeld met mondkapjes om zich te beschermen tegen luchtverontreiniging.
- (1p) Welke scheidingsmethode wordt hier gebruikt?
- (1p) Tegen welk soort luchtverontreiniging beschermen
deze kapjes?
- (1p) Tegen welke soort luchtverontreiniging beschermen
deze kapjes niet?
- (1p) Een gasmasker beschermt ook tegen sommige gevaarlijke gassen. Hoe doet een gasmasker dat?
-
(1p) Waarom moet de vulling van een gasmasker na verloop van tijd vernieuwd worden?
-
(1p) Een stuk papier is vochtig geworden en wordt gedroogd in de zon. Met welke scheidingsmethode is het drogen van het papier vergelijkbaar? Kies uit: adsorberen, bezinken, destilleren, extraheren, filtreren of indampen.
|
§5 Water zuiveren
In de laatste paragraaf gaan we het hebben over het zuiveren van water tot drinkwater.
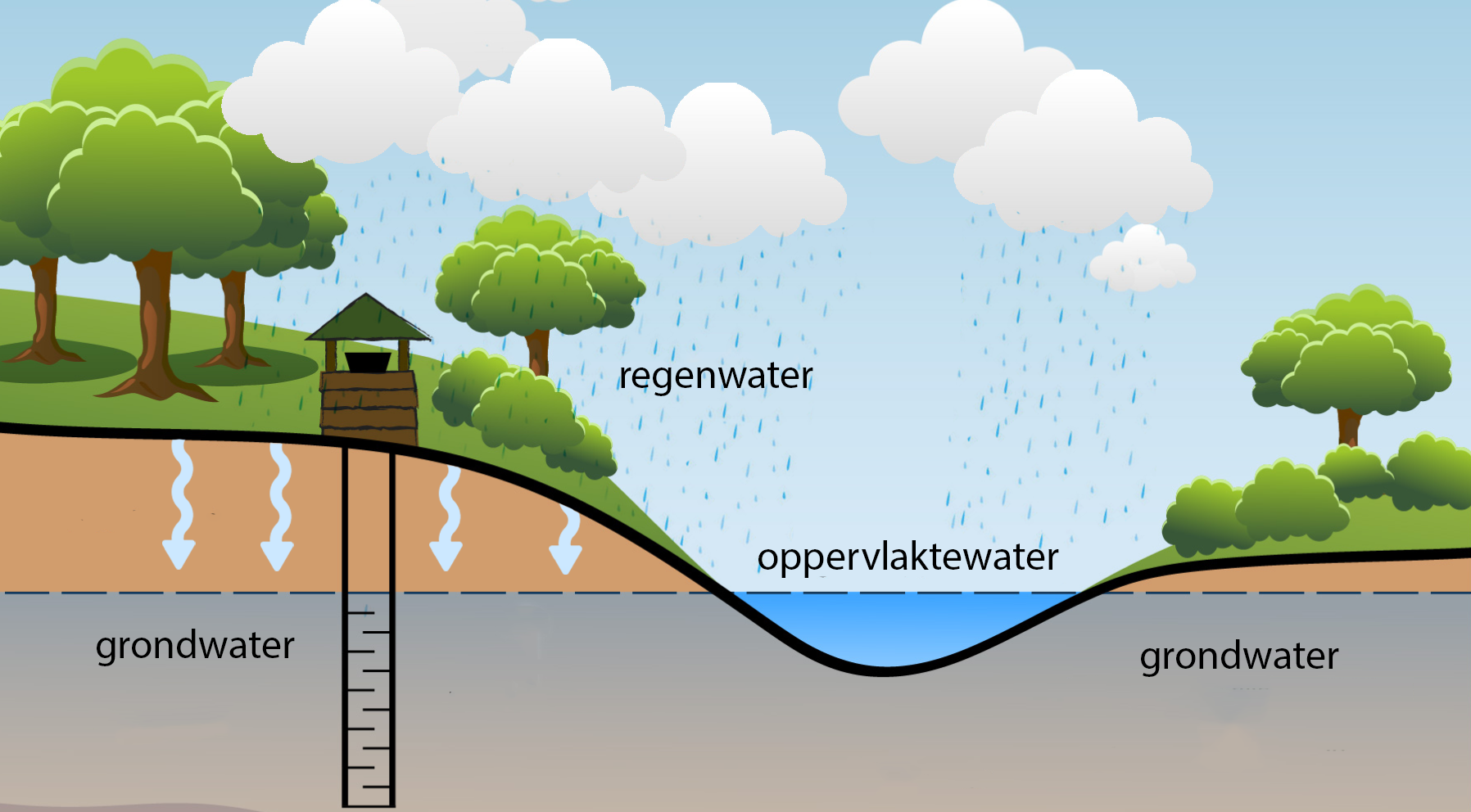
Drinkwater komt in Nederland uit zowel oppervlaktewater als grondwater. Oppervlaktewater bevindt zich aan het aardoppervlak. Denk bijvoorbeeld aan meren en rivieren. Grondwater bevindt zich letterlijk onder de grond, bijvoorbeeld in zandlagen. Grondwater is vaak afkomstig uit regenwater dat eerst oppervlaktewater vormde, maar daarna tientallen tot honderden meters de grond in zakt (zie de onderstaande afbeelding). Grondwater is over het algemeen zuiverder dan oppervlaktewater. Dit komt doordat het door de grondlagen gefilterd is.
Oppervlakte- of grondwater kan in een waterzuiveringsinstallatie worden gezuiverd tot drinkwater. Dit gebeurt in een aantal stappen. Hieronder vind je een aantal veelvoorkomende stappen:
- Met filters worden grove stukjes vuil uit het water gehaald.
- Door het water in aanraking te laten komen met lucht, zal een deel van het opgeloste ijzer in het water reageren met zuurstof. Hierbij ontstaan kleine vaste stukjes ijzeroxide. Deze stukjes kunnen daarna bezinken of weggefilterd
- Een stof als natronloog kan worden toegevoegd om een aantal andere opgeloste stoffen in het water als vaste stoffen te laten neerslaan.
- Ziektekiemen kunnen onschadelijk worden gemaakt met bijvoorbeeld chloor, ozon of UV-straling.
- Daarnaast zijn er actieve koolfilters die de laatste geur- en smaakstoffen verwijderen.
Het resultaat is schoon drinkwater. Zoals je eerder in dit boek geleerd hebt, is dit geen zuiver water. Er zitten nog steeds hele kleine hoeveelheden opgeloste stoffen in.
De vijf stappen van de hierboven beschreven zuivering zijn hieronder weergegeven in een zogenaamd blokschema. Blokschema's komen geregeld voor in toetsen en examens, dus het is van belang dat je dit soort afbeeldingen goed kan aflezen. De blokken in de afbeelding staan voor verschillende processen die plaatsvinden. De pijlen geven aan of stoffen worden toegevoegd of juist worden afgevoerd.
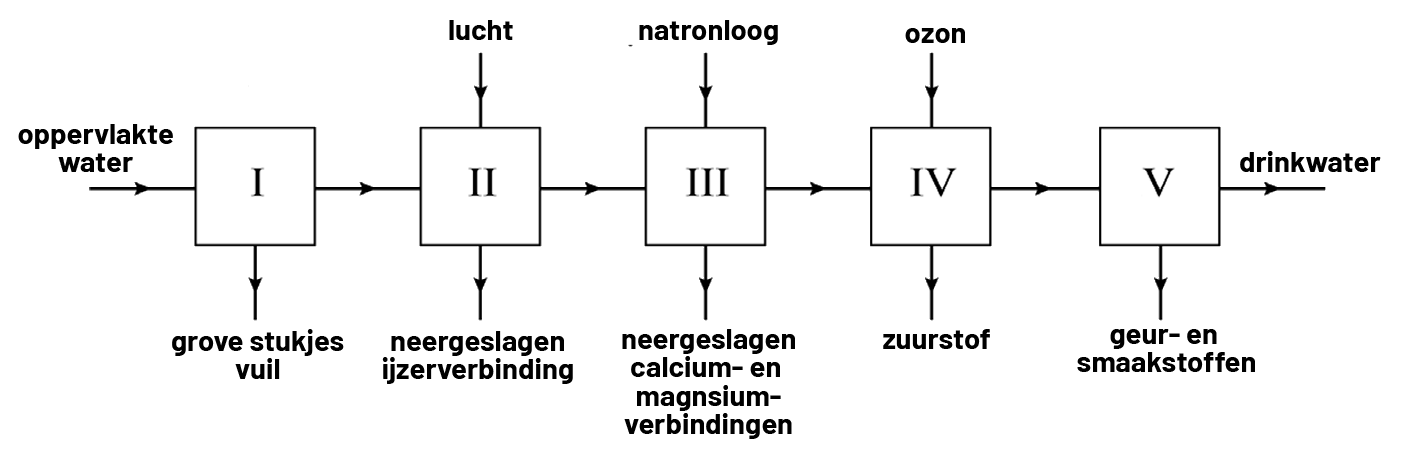 (Design schema: examen nask 2)
(Design schema: examen nask 2)
Op plekken op aarde waar zoetwater niet aanwezig is, wordt zeewater in drinkwater omgezet. Dit is echter lastiger, door de grote hoeveelheid keukenzout (NaCl) die hierin opgelost is. Met behulp van destillatie kan het water in dat geval van het zout gescheiden worden. Het destillaat is dan schoon water en het residu is zout.
Regenwater zou ook nog gebruikt kunnen worden voor drinkwater. Regenwater is vrij zuiver, omdat het ontstaan is bij het verdampen van oppervlaktewater. Dit werkt als een soort destillatieproces. Het water verdampt, terwijl de stoffen in het water achterblijven. Er kunnen wel nog zwaveldioxide (SO2) en verschillende soorten stikstofoxiden (NOx) in het water zitten (hierover in een later hoofdstuk meer). Dit maakt regenwater lichtelijk zuur.
 Leerdoelen:
Leerdoelen:
|
- Zorg dat je het verschil begrijpt tussen oppervlaktewater, grondwater, regenwater en drinkwater.
- Zorg dat je weet hoe scheidingsmethoden zoals filtratie, bezinken en adsorptie worden gebruikt bij het zuiveren van water.
- Zorg dat je blokschema's kan aflezen.
|
 Opdrachten
Opdrachten
|
- (1p) Leg uit waarom grondwater over het algemeen zuiverder is dan oppervlaktewater.
-
Hieronder is een blokschema weergegeven dat hoort bij een bepaald type drinkwaterinstallatie:
 (Design schema: examen nask 2)
(Design schema: examen nask 2)
- (1p) Leg uit welke scheidingsmethode waarschijnlijk is ingezet in blok I.
- (1p) Tijdens proces II en III vormen vaste stukjes ijzeroxide, calcium- en magnesiumverbindingen. Noem twee scheidingsmethoden waarmee deze deeltjes verwijderd kunnen worden.
- (1p) Leg uit welke scheidingsmethode waarschijnlijk is ingezet in blok V. Leg je antwoord uit.
-
In Friesland wordt water uit de bodem opgepompt om er drinkwater van te maken. Het opgepompte water bevat nog ongewenste stoffen en is lichtgeel van kleur. Het drinkwater wordt daarom gezuiverd via onder meer de volgende stappen:
1 - Water wordt uit de bodem opgepompt.
2 - Het opgepompte water wordt in contact gebracht met veel lucht. Sommige stoffen die vies smaken, zoals ijzerverbindingen, vormen daarbij vlokjes.
3 - Het vloeibare mengsel wordt gezeefd in bakken die gevuld zijn met fijn zand. De vlokjes blijven achter.
4 - Met de stof natronloog worden calciumionen en magnesiumionen in het water omgezet tot calciumhydroxide en magnesiumhydroxide. Deze stoffen slaan neer en worden vervolgens verwijderd.
5 - Daarna worden de stoffen verwijderd die de lichtgele kleur veroorzaken. Hierbij wordt een koolfilter gebruikt.
Ten slotte wordt het gereinigde water het leidingnet ingepompt.
- (1p) Vóórdat het water wordt opgepompt (vóór stap 1) wordt het water steeds anders genoemd. In welke volgorde verandert deze naam?
A: grondwater - oppervlaktewater - regenwater
B: grondwater - regenwater - oppervlaktewater
C: regenwater - oppervlaktewater - grondwater
D: regenwater - grondwater - oppervlaktewater
- (1p) Leg uit hoe in stap 2 lucht ervoor kan zorgen dat ijzer uit het water wordt gehaald.
-
(2p) Geef aan op welk verschil in stofeigenschap stap 3 berust. En om welke scheidingsmethode gaat het hier?
-
(2p) Wat gebeurt er in een koolfilter met de stoffen die de kleur in het water veroorzaken (stap 5)? En om welke scheidingsmethode gaat het hier?
(Bron: Examen VMBO-T, 2023-1)
-
Levulinezuur (C5H8O3) kan worden gebruikt voor het produceren van nylon en wordt gemaakt uit pulp (gemalen afvalhout). In onderstaand blokschema is het proces waarbij levulinezuur wordt verkregen vereenvoudigd en onvolledig weergegeven.

In ruimte I treden meerdere reacties op. Bij één van deze reacties ontstaat methaanzuur en levulinezuur. Het methaanzuur wordt afgevoerd. In ruimte II worden de pulpresten door middel van filtratie verwijderd uit het mengsel dat in ruimte I is ontstaan. In ruimte III wordt vervolgens een zwavelzuuroplossing afgescheiden met behulp van een oplosmiddel waarin alle stoffen oplossen, behalve de zwavelzuuroplossing. In ruimte IV wordt ten slotte het levulinezuur verkregen door middel van destillatie.
- (1p) Bij het filtreren in ruimte II wordt gebruikgemaakt van een verschil in stofeigenschap. Welke stofeigenschap?
- (2p) Geef de naam van de scheidingsmethode die gebruikt wordt in ruimte III. En van welk verschil in stofeigenschap wordt hier gebruik gemaakt.
- (3p) Bij de destillatie (ruimte IV) wordt een 'kolom' gebruikt. Deze is hieronder afgebeeld.
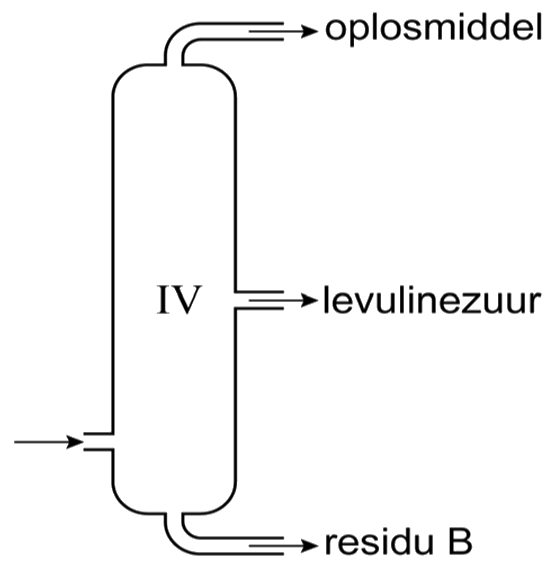
Welke van onderstaande kenmerken heeft destilleren met behulp van een kolom? Geef bij elk van de volgende stellingen aan of ze correct zijn:
- De stof met het laagste kookpunt verdampt het eerst.
- Onderin de kolom is de temperatuur het laagst.
- De stof met het laagste kookpunt komt onder uit de kolom.
-
(2p) Uit het blokschema blijkt dat twee stoffen kunnen worden hergebruikt in dit proces. Geef de namen van deze twee stoffen. Kies uit: levulinezuur, zwavelzuur, methaanzuur en oplosmiddel.
|
| BINAS: |
|
| 15-17 |
Dichtheid, smeltpunt en kookpunt van verschillende stoffen |
 Leerdoelen:
Leerdoelen:
 Opdrachten
Opdrachten

 (Afbeelding: Tummers77; CC BY-SA 4.0)
(Afbeelding: Tummers77; CC BY-SA 4.0)

 Leerdoelen:
Leerdoelen:
 Opdrachten
Opdrachten


 EXPERIMENT
EXPERIMENT
 (Afbeelding: SirVir; CC BY-SA 3.0)
(Afbeelding: SirVir; CC BY-SA 3.0)

 Leerdoelen:
Leerdoelen:
 Opdrachten
Opdrachten

 (Afbeelding: Pixabay; PD)
(Afbeelding: Pixabay; PD)

 (Afbeelding: Ravedave; CC BY 2.5 / SomnathWiki007; CC BY 4.0)
(Afbeelding: Ravedave; CC BY 2.5 / SomnathWiki007; CC BY 4.0)


 EXPERIMENT
EXPERIMENT
 Leerdoelen:
Leerdoelen:
 Opdrachten
Opdrachten

 (Design schema: examen nask 2)
(Design schema: examen nask 2)
 Leerdoelen:
Leerdoelen:
 Opdrachten
Opdrachten



