Met de theorie uit de vorige paragraaf kunnen we het begrijpen wanneer we stoffen kunnen ontleden in twee of meerdere andere stoffen.
Als we veel energie aan een stof toevoegen, dan kan het gebeuren dat er een chemische reactie optreedt. De stof kan hierbij opsplitsen in twee of meerdere stoffen. We noemen een dergelijke reactie een ontledingsreactie. Stoffen die we kunnen ontleden noemen we ontleedbare stoffen. Stoffen die we niet kunnen ontleden noemen we niet-ontleedbare stoffen.
Suiker kunnen we bijvoorbeeld ontleden in koolstof en water (zie het onderstaande filmpje).
De koolstof die ontstaat, kunnen we niet verder ontleden, maar het water wel. Als we water onder stroom zetten, dan ontleed het in zuurstof en waterstof. Zuurstof en waterstof kunnen we niet verder ontleden (zie de onderstaande afbeelding).
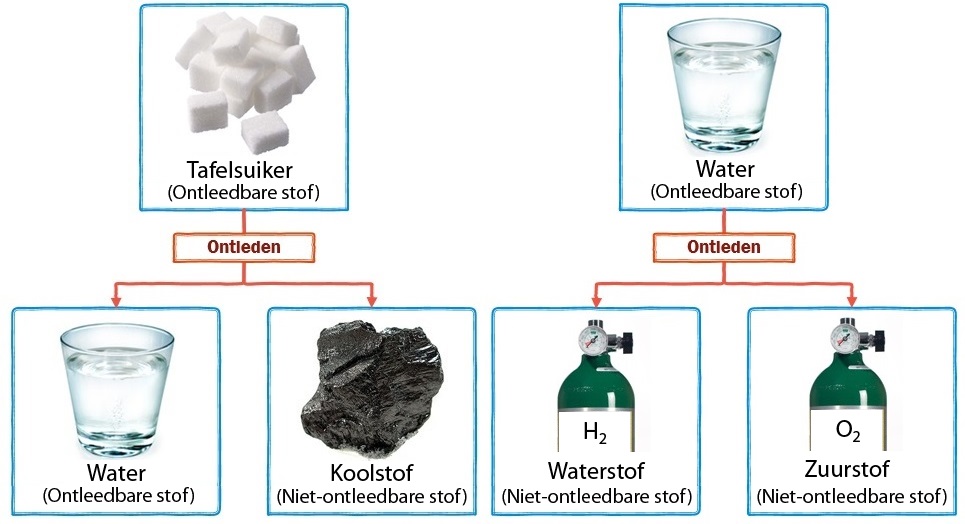
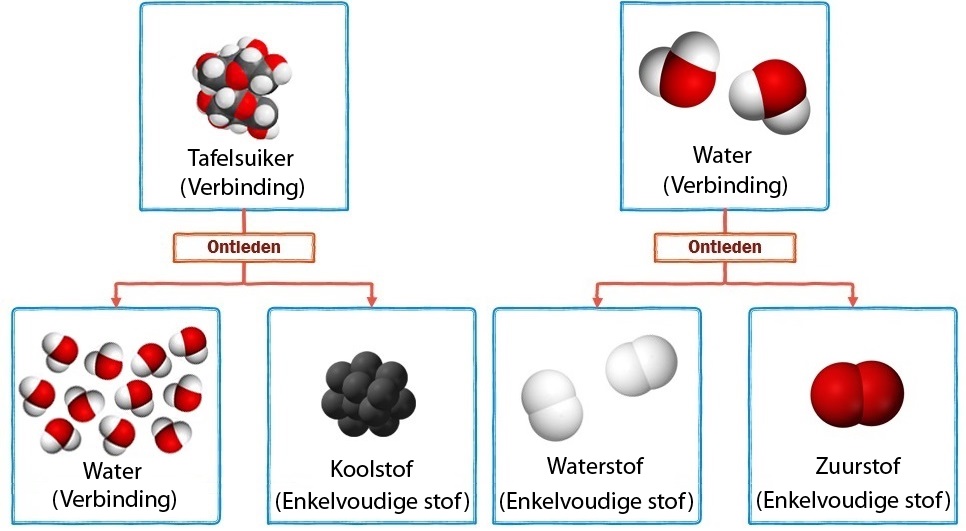
In de onderstaande afbeelding zien we dezelfde reactie op moleculair niveau. Merk op dat de ontleedbare stoffen uit meerdere soorten atomen bestaan. We noemen dit type stoffen ook wel verbindingen. De niet-ontleedbare stoffen bestaan uit slechts één soort atoom. We noemen dit type stoffen ook wel enkelvoudige stoffen of elementaire stoffen. Bij ontleden worden de verschillende soorten atomen dus van elkaar losgetrokken.
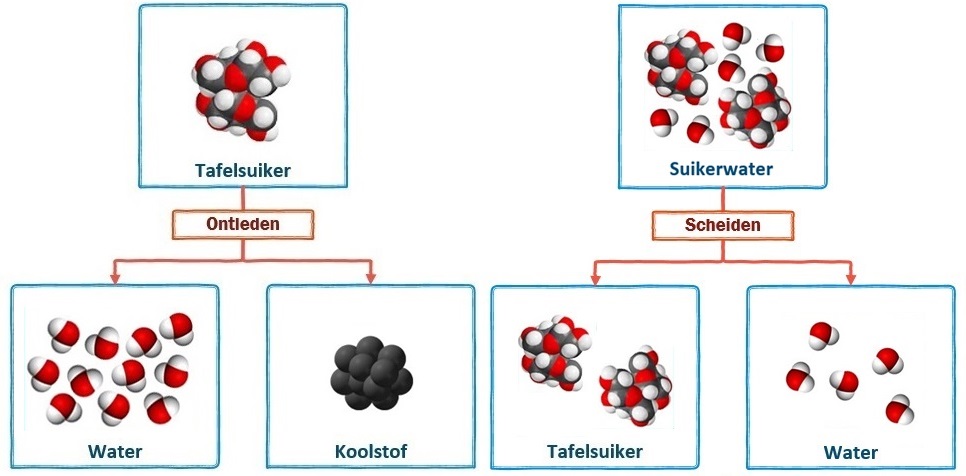
Hieronder zien we links de ontleding van suiker in koolstof en water en rechts het scheiden van suikerwater in water en suiker. Bij ontleden ontstaan nieuwe moleculen en dus nieuwe stoffen. Dit is dus een chemische reactie. Suikerwater daarentegen is een mengsel. Mengsel bestaan uit meerdere soorten moleculen. Tijdens het scheiden ontstaan geen nieuwe moleculen, maar worden de moleculen alleen gesorteerd. Hier heeft dus geen chemische reactie plaatsgevonden.
-
-
Je hebt een onbekende moleculaire vloeistof.
- Na het uitvoeren van een experiment blijkt dat deze vloeistof een zuivere stof is. Vertel hoe dit experiment gedaan is.
- Na het uitvoeren van een ander experiment blijkt dat de vloeistof ook een enkelvoudige stof is. Vertel hoe dit experiment gedaan is.
- Leg uit hoeveel soorten atomen en hoeveel soorten moleculen deze vloeistof bevat.
- Leg uit of er bij de volgende processen sprake is van ontleding of scheiding:
- Zout wordt gewonnen door zeewater te laten verdampen.
- Aardgas wordt verbrand in de brander.
- Alcohol wordt gedestilleerd uit wijn.
- Vlees verkoolt op een barbecue.
- In de industrie maakt men chloor uit natriumchloride (keukenzout).
- Je kunt water koken en je kunt water ontleden.
- Wat ontstaat er bij het koken van water?
- Wat ontstaat er bij het ontleden van water?
- Leg uit in welk geval er een chemische reactie plaatsvindt.
- Leg uit voor welk proces je meer energie nodig hebt.
 Begrijpen van het verschil tussen ontleden en scheiden, mengsels en zuivere stoffen
Begrijpen van het verschil tussen ontleden en scheiden, mengsels en zuivere stoffen